多克隆抗体的制备以及佐剂在其制备中的应用
一、抗体
抗体是地球生命进化史上一类不寻常的蛋白质,是生物医学界的 “魔力子弹”,在哺乳动物中,抗体能对机体固有的免疫系统起到增强和补充作用,当机体遭遇外界刺激(如细菌、病毒或其他病原微生物等)时,会产生获得性免疫反应,合成并分泌抗体。
抗体是宿主蛋白质,在体内存在外来分子时产生,它们主要由浆细胞合成,浆细胞是B淋巴细胞谱系中终分化的细胞,并在血液和淋巴中循环,与外来抗原结合。随后,抗体-抗原复合物主要通过巨噬细胞的吞噬作用从循环中移除。抗体具有重要的结构和功能特征,在功能上,能够结合抗原和免疫系统的特定细胞或蛋白质,在结构上,抗体由一个或多个“Y”形组成,每个“Y”含有四种多肽,两种相同的重链多肽和两种相同的轻链多肽。根据“Y”型的数量和它们包含的重链多肽的类型分为五类,即IgG、IgM、IgA、IgE和IgD,其中IgG在血清中的含量丰富。
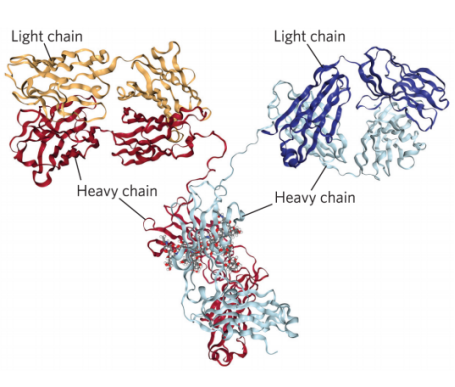
二、多克隆抗体
由于抗原分子具有多种抗原决定簇,每一种决定簇可激活具有相应抗原受体的B细胞产生免疫应答,因而可产生多种针对不同抗原决定簇的抗体,这些由不同B细胞克隆产生的抗体称之为多克隆抗体。
多克隆抗体作为一种重要工具被广泛应用于科学研究和诊断中,它们能够识别特定的抗原物质,可以应用于Western blot、放射性免疫测定、ELISA、直接-间接荧光抗体检测、红细胞凝集试验、免疫组化(IHC)、免疫沉淀(IP)、免疫扩散、亲和层析、酶学、基因分离等众多实验中。用途极其广泛。
高亲和性多克隆抗体能够同时识别抗原上的多个表位,通过多价结合的协同效应大幅提升抗原抗体复合物的稳定性。这种特性在Western Blot(WB)和ELISA等实验中尤为关键,多表位结合能够有效放大信号并减少漏检的风险,亲和性低的抗体会因结合能力弱而导致信号捕获不足而出现假阴性的结果。而且高亲和性抗体对靶蛋白的微小结构变化(如糖基化、部分变性)具有更高容忍度,在免疫组化(IHC)等实验中对构象变化的抗原仍能稳定结合,低亲和性抗体对表位构象敏感,抗原轻微改变即可导致结合失效。多克隆抗体的高亲和性是其核心优势,是保障检测灵敏度和实验稳定性的基石,稳固的结合能力不仅能够提升低丰度靶标的检出率,还赋予了实验体系更强的抗干扰能力
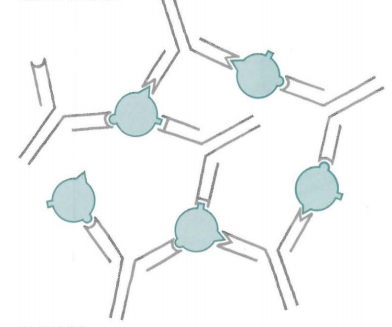
多克隆抗体与多价抗原结合
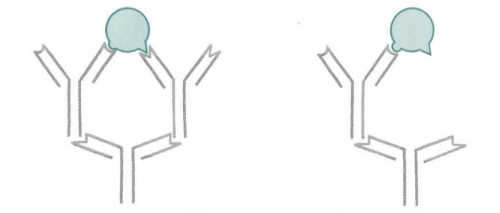 低亲和力 高亲和力
低亲和力 高亲和力
三、动物选择
实验动物选择是制备多克隆抗体制备是否能达到预期的关键因素之一,广泛的脊椎动物物种可用于生产抗血清,如:兔子、小鼠、羊、马、驴、猪等。其中兔子是常规生产多克隆血清的一个很好的选择。动物的选择主要根据抗原的生物学特性和所需获得抗体的数量和用途,如制备抗γ-免疫球蛋白抗血清,多用兔子和山羊,因动物反应良好,且能够提供足够数量的血清。
抗原与动物种属之间的关系一般认为抗原的来源与免疫动物的亲缘关系越远,免疫原性越强,产生抗体的效价越高。而同种系或亲缘关系较近者,产生抗体的效价低,甚至不产生抗体。比如:针对小鼠抗原的抗体反应可能在小鼠或大鼠中不发挥作用,但是在兔中就可以。免疫亲缘关系较远的哺乳动物可产生高达10mg/mL的抗体,但如果免疫同种异型动物,产生的抗体量低于1mg/mL,鸡经常被用来制备IgY(等同于哺乳动物的IgG)的多克隆抗体,而且IgY不会和哺乳动物IgG发生交叉反应。
1. 小鼠:小鼠是啮齿目中体型较小的动物。新生小鼠1.5g左右,21天断乳时12~
15g,1.5至2月龄体重达20g以上,可供实验使用。
2. 兔:兔耳大,表面分布有清晰的血管。有特殊的血清型和唾液型,血清型分为α'、β'、α'β'和 O 型四种。由于抗原刺激机体后,体液免疫应答反应强烈,所以兔被广泛用于制备高效价的特异性强的免疫血清。应选择年龄在6个月以上,体重以2~3kg为宜。

3.  羊:可用于生产多种抗血清,优先选择成年个体(免疫系统成熟),健康状态良好的羊。
羊:可用于生产多种抗血清,优先选择成年个体(免疫系统成熟),健康状态良好的羊。
4. 豚鼠:选择成年(3个月以上)且健康的豚鼠(体重200-250g),此时免疫系统成熟,免疫后产生的抗体效价较高。

四、抗原选择
能被特异性免疫应答所识别的分子被称为抗原。然而,不是所有的抗原都是免疫原。免疫原是指能引起体液免疫和(或)细胞免疫的分子。如大多数蛋白质、细菌、病毒等。分子量大于5KDa的抗原更易于刺激抗体产生,一些小分子物质(半抗原)如小的多肽、多糖、类脂和某些药物等,只有在和有活性的大分子物质(载体,如BSA、OVA)偶联时才能引起免疫应答。能引起抗体应答的抗原必定是免疫原。自然界中的抗原物质种类繁多,包括各种天然抗原、人工抗原、合成抗原、基因工程抗原等,绝大多数的天然抗原不是单一成分,在制备抗体时需要进行纯化。一般而言,大多数动物的免疫系统是非常敏感的,用于免疫的抗原建议是纯化品,抗原经12.5%的PAGE电泳后,仅出现一条区带,即认为可作为免疫用抗原。
不同动物种类对同一抗原有不同的免疫应答表现,因此对不同性质的抗原选用的动物也不相同。蛋白质抗原一般适用于大多数动物,常用的有兔和羊,但在某些动物体内因为有类似物质或其他的原因,蛋白质抗原对这些动物免疫原性极差,如兔子对胰岛素、绵羊对IgE、山羊对多种酶类均不易产生抗体。甾体激素多选用兔,酶多选用豚鼠。
五、佐剂应用
免疫佐剂是指预先或与抗原同时注入体内,可增强机体对抗原的免疫应答或改变免疫应答类型的非特异性免疫增强性物质,其目的是为了提高抗原对机体的免疫原性,提高机体产生抗体的效价。与仅使用抗原相比,其抗体的产量会更大。油性免疫佐剂介导的放大效应包括:(1)一种免疫原的仓库,使其能在较长时间内缓慢释放从而向免疫系统提呈;(2)免疫刺激被优化,一般免疫刺激剂和抗原集中于同一微环境中,并同时与抗原提呈细胞和淋巴细胞相互作用;(3)免疫系统细胞非特异性活化,而这种活化对产生抗体的反应有益。
目前动物免疫中应用广泛的是弗氏佐剂和其它的一些油性佐剂,如:弗氏不完全免疫佐剂(加强型)、弗氏完全免疫佐剂(加强型)、乳化型快速完全免疫佐剂和乳化型快速不完全佐剂等,完全佐剂由不完全佐剂加卡介苗组成。由于都是油剂,因此在免疫动物时,建议先将佐剂与抗原按合适的体积比混匀,制成油包水型乳化液。初次免疫一般用完全佐剂,刺激机体产生较强的免疫应答;再次免疫时,使用不完全佐剂。弗氏不完全免疫佐剂(加强型)、弗氏完全免疫佐剂(加强型),乳化型快速完全免疫佐剂和乳化型快速不完全佐剂,是商品化的高效的佐剂之一。特别适合单抗研发用小鼠的免疫以及兔子、山羊、豚鼠等多克隆抗血清的制备。

在免疫动物前,应先将弗氏不完全免疫佐剂(加强型)、弗氏完全免疫佐剂(加强型)、乳化型快速完全免疫佐剂或乳化型快速不完全佐剂等油性佐剂与抗原按一定比例混合,制备成“油包水”乳状液。可溶性抗原和免疫佐剂在乳化过程中,含有抗原的小水滴被油所捕获,在非常黏的乳剂中形成颗粒,传统的乳化方法有研磨法、注射器混合法、超声法。这些方法抗原损耗大、用时长且不易操作。可以用手持移液器式佐剂乳化器进行乳化,乳化过程操作简单、方便快捷、安全性高、用时少,几分钟就可乳化完全,且抗原几乎无损耗。乳化器如下图:

 乳化器乳化具体操作方法有2种:(1)将佐剂先加入乳化管,然后加少部分抗原搅拌乳化几下后再加抗原继续乳化,直到抗原加完再乳化几分钟即可。(2)抗原和佐剂加入乳化管,稍等抗原会沉入底部和佐剂分层,用搅拌器自上而下慢慢搅拌佐剂入抗原层,慢慢下移这时会发现混合液很快乳白越来越粘,几分钟就可完成。乳化示意图如下:
乳化器乳化具体操作方法有2种:(1)将佐剂先加入乳化管,然后加少部分抗原搅拌乳化几下后再加抗原继续乳化,直到抗原加完再乳化几分钟即可。(2)抗原和佐剂加入乳化管,稍等抗原会沉入底部和佐剂分层,用搅拌器自上而下慢慢搅拌佐剂入抗原层,慢慢下移这时会发现混合液很快乳白越来越粘,几分钟就可完成。乳化示意图如下:
乳化完成后,将一滴乳剂滴入水中,若保持完整不分散,成滴状浮于水面,则为乳化完全,为合格的油包水剂。各成分在乳化后不会分散,在运用到宿主组织后,才能发挥抗原仓库的作用。如下图:

弗氏不完全免疫佐剂(加强型)、弗氏完全免疫佐剂(加强型)、乳化型快速完全免疫佐剂和乳化型快速不完全佐剂的使用比例是30~50%。接近30%乳化粘度增加,接近50%乳化粘度减小。因此建议夏季使用低浓度冬季使用高浓度乳化,这样既能得到很好的免疫效果也能减少注射时带来的阻力困难。
六、免疫动物
1. 免疫剂量
一般而言,需要纳克到微克级的抗原加上佐剂才能诱导高滴度的抗体反应,例如,兔需要免疫500~1000μg,小鼠需要10~200μg,山羊或者绵羊需要250~5000μg可溶性抗原加上乳化型快速完全免疫佐剂能诱发高滴度的抗体反应。越小的动物需要的抗原/佐剂混合物的浓度越低,但是产生抗体所需的抗原剂量并不一定必须要根据动物的大小而增加或减少。可能一只4kg的兔需要的抗原剂量同25g小鼠所需的一样。抗原的剂量非常关键,高剂量的抗原导致低亲和力的B细胞活化,而低剂量抗原能引起高亲和力的B细胞活化。佐剂的应用使低剂量抗原进行免疫成为可能,佐剂能提高抗体滴度,并能减少免疫耐受产生的机会。
2. 免疫途径
抗原的进入途径决定了抗原吸收、分布和代谢的速度,吸收越快,分解代谢越快,对机体的影响时间越短。吸收越快,单位时间内的有效抗原量就越大,机体的免疫应答就越强,不良反应也越强。应根据不同抗原及实验要求选择不同的免疫途径。免疫途径包括皮内注射、皮下注射、淋巴结内注射、腹腔注射、静脉注射、肌内注射及脾内注射等途径。可溶性抗原(糖蛋白、脂蛋白、酶类、补体、细菌外毒素、多糖和核酸等)及抗原量少的情况下,一般多采用添加免疫佐剂,如完全免疫佐剂和不完全佐剂,在淋巴结内或淋巴结周围或足垫、皮内、皮下多点注射的方式;颗粒性抗原(各种动物细胞抗原、细菌抗原和寄生虫抗原等)及抗原量多的情况下,可不添加佐剂,直接采用静脉、腹腔、肌内注射的方式。也可以根据具体情况,联合不同的免疫途径制备高效价抗体。
3. 免疫方法(以兔子为例)
(1) 皮下注射:
从靠近颈部后侧的一侧开始,用拇指和食指捏住皮肤。将皮肤从身体上拉开,将针插入已形成的空隙中。将针的末端从一侧向另一侧移动一小段距离,以确保它不会插入肌肉或身体壁。按下活塞以注射所需的量。暂停几秒钟。当针头被拔出时,应用食指和拇指轻轻按压注射部位,防止接种液外渗。如下图:
(2)肌内注射
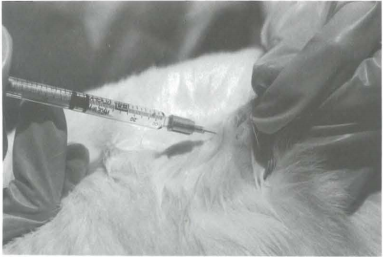
将兔子从笼子里取出,放在足够粗糙的钢丝或固体表面上,让兔子感到舒适。应避免让兔子置于光滑的表面上,因为兔子会在任何光滑的表面上收缩肌肉。
注射通常在后腿的大腿肌肉中进行。从前部抓住腿,将注射器插入大腿肌肉靠近髋部的后部。将针插入肌肉,轻轻尝试抽回活塞。如果遇到阻力,可以继续进行注射。如果出现血液,说明针头误入腿上的小静脉或动脉。拔出注射器,移动到附近的部位并再次尝试。抗原应缓慢、平稳地注入。注射完成后拔出针头,轻轻按摩注射部位。如下图:
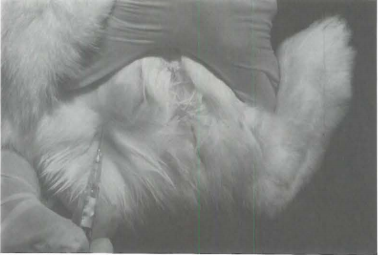
(3)皮内注射
皮内注射在较大动物的免疫接种中相当常见。与肌内注射一样,皮内注射用于以非常缓慢的速度释放免疫原。接种物被注射在皮肤层之间,并缓慢吸收进入体内。
注射部位可选择胁部高位(肋骨与髋骨之间)或背部区域。剃除适当大小的区域以露出皮肤,用食指和拇指夹住皮肤,确认针头与注射器连接紧密。针头斜面朝上,轻微刺入皮下后继续在皮层间平行推进至少0.5~0.7厘米。接种液应在皮下形成致密性疱疹,拔针时用指腹压闭针道,




 豫公网安备 41031102000387号
豫公网安备 41031102000387号